Όπως ανακοίνωσαν οι φαρμακευτικές εταιρείες Sanofi και Regeneron Pharmaceuticals, Inc. η Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA), εξέδωσε θετική γνωμοδότηση για τη χορήγηση άδειας κυκλοφορίας στο dupilumab, προτείνοντας την έγκρισή του στην Ευρώπη για χρήση σε ενήλικες ασθενείς με μέτρια έως σοβαρή ατοπική δερματίτιδα, οι οποίοι έχουν κριθεί κατάλληλοι για να λάβουν συστηματική θεραπεία.
Η ατοπική
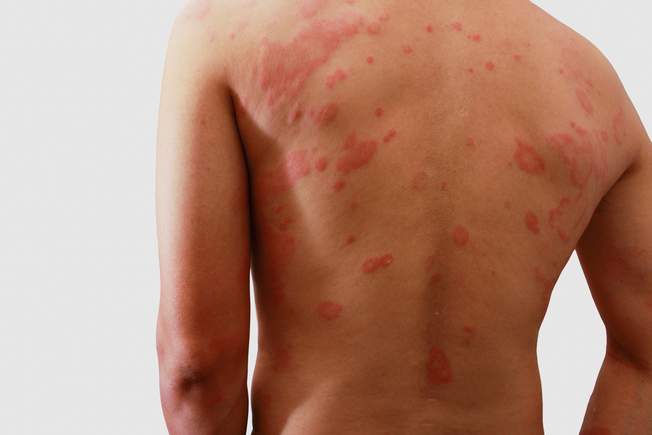
δερματίτιδα, μία μορφή εκζέματος, αποτελεί μία χρόνια φλεγμονώδη νόσο με
συμπτώματα που συχνά εμφανίζονται ως εξάνθημα στην επιφάνεια του δέρματος. Η
μέτρια έως σοβαρή ατοπική δερματίτιδα χαρακτηρίζεται από εξανθήματα, που συχνά
καλύπτουν μεγάλο τμήμα του σώματος, και είναι δυνατό να συνοδεύονται από
έντονο, επίμονο κνησμό και ξηρότητα, σκάσιμο, ερυθρότητα, δημιουργία εφελκίδων
και εξιδρώματος. Ο κνησμός είναι ένα από τα πιο δύσκολα συμπτώματα των ασθενών
και μπορεί να είναι εξουθενωτικός. Επιπρόσθετα, οι ασθενείς με μέτρια έως
σοβαρή ατοπική δερματίτιδα παρουσιάζουν υψηλού βαθμού διαταραχές ύπνου, καθώς
και συμπτώματα αυξημένου άγχους και κατάθλιψης εξαιτίας της νόσου.
Το dupilumab είναι ένα ανθρώπινο μονοκλωνικό αντίσωμα που έχει σχεδιαστεί για να αναστέλλει ειδικά την υπερενεργή σηματοδότηση δύο βασικών κυτοκινών, της IL-4 και της IL-13, που θεωρείται ότι αποτελούν σημαντικό παράγοντα της επίμονης υποκείμενης φλεγμονής στην ατοπική δερματίτιδα.
Εφόσον
εγκριθεί, το dupilumab θα είναι διαθέσιμο σε προγεμισμένη σύριγγα που μπορεί να
χορηγηθεί από τον ίδιο τον ασθενή κάθε δεύτερη βδομάδα μετά την αρχική δόση. Το
dupilumab μπορεί να χρησιμοποιείται με ή χωρίς τοπικά κορτικοστεροειδή.
Η Ευρωπαϊκή Επιτροπή αναμένεται να λάβει την οριστική απόφαση για την Έγκριση της 'Aδειας Κυκλοφορίας (MAA) του dupilumab στην Ευρωπαϊκή Ένωση τους επόμενους μήνες. Η γνωμοδότηση της Επιτροπής Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) βασίζεται σε στοιχεία από μελέτες του παγκόσμιου κλινικού προγράμματος για την ατοπική δερματίτιδα LIBERTY, το οποίο περιλαμβάνει τις κλινικές μελέτες SOLO 1, SOLO 2, SOLO-CONTINUE,CHRONOS και CAFÉ. Αυτές οι μελέτες συμπεριλαμβάνουν δεδομένα από σχεδόν 3.000 ενήλικες ασθενείς με μέτρια έως σοβαρή ατοπική δερματίτιδα οι οποίοι δεν ελέγχονταν επαρκώς με συνταγογραφούμενες θεραπείες τοπικής εφαρμογής ή ανοσοκατασταλτικά φάρμακα, όπως η κυκλοσπορίνη, ή στην περίπτωση που οι συγκεκριμένες θεραπείες δεν ενδείκνυνται.











